MEKANISME REAKSI ADISI PADA ALDEHID DAN KETON
Gugus karbonil sangat terpolarisasi, sehingga elektrofil
menyerang atom oksigen dan nukleofil menyerang atom karbon. Salah satu
reaksi terpenting yang dimasuki aldehida dan keton adalah adisi
nukleofilik ke gugus karbonil:

Kita dapat menulis
mekanisme umum berikut:
Adisi nukleofilik H2O
H2O dapat berperilaku sebagai nukleofil, meskipun nukleofilisitasnya tidak
sekuat OH-. Dalam larutan air, terdapat kesetimbangan antara senyawa karbonil
dan diol geminal yang sesuai , yang juga dikenal
sebagai karbonil hidrat :

Hidrat karbonil hanya terbentuk
perlahan dalam air pada pH 7, tetapi terbentuk jauh lebih cepat dengan adanya
asam atau basa. Oleh karena itu, reaksi dikatalisis oleh asam atau basa -
konstanta kesetimbangan tetap sama, tetapi reaksi mencapai posisi kesetimbangan
lebih cepat.
katalisis
Dalam kasus katalisis
basa, pada pH> 7, OH - hadir, yang merupakan nukleofil
yang jauh lebih baik daripada air:
Penambahan katalis basa
Dalam mekanisme katalis
basa, ion hidroksida bertindak sebagai nukleofil. Air kemudian menjebak
hasil tambahan antara dengan pembentukan diol geminal, katalis dilepaskan lagi.
Dalam mekanisme katalis
asam, protonasi ke basa Lewis karbonil-O terjadi lebih dulu. Hal ini
membuat gugus C = O lebih terpolarisasi dan gugus atom karbonil C menjadi
elektrofil yang lebih kuat. Sekarang sebuah molekul air, meskipun masih
merupakan nukleofil lemah, menyerang dengan sangat cepat:
Penambahan Katalis Asam
Proses katalis basa lebih cepat karena ion OH - adalah
nukleofil yang jauh lebih baik daripada molekul air. Sebaliknya, proses
katalis asam lebih cepat karena protonasi gugus karbonil menciptakan elektrofil
yang lebih baik untuk serangan nukleofil.
Persamaan reaksi
menunjukkan bahwa hidrasi aldehida dan keton bersifat reversibel. Kesetimbangan
biasanya di sebelah kiri untuk keton dan di sebelah kanan untuk formaldehida
dan aldehida dengan substituen penarik elektron. Aldehida memiliki
konstanta kesetimbangan sekitar 1, misalnya
Secara umum, penambahan
gugus C = O berlangsung lebih cepat, semakin elektrofilik atom karbonil C:
Urutan reaktivitas gugus
C = O dalam adisi nukleofilik:
Kekuatan elektrofilik
dari pusat ini secara kasar dapat dikorelasikan dengan stabilitas ion karbenium
yang diformulasikan dalam struktur resonansi dipolar. Ion karbenium yang
lebih tersubstitusi (dengan gugus alkil) lebih stabil, dan reaktivitasnya menurun
dalam urutan itu. Substituen penarik elektron mendestabilisasi atom karbon
yang terpolarisasi secara positif, itulah sebabnya ia lebih reaktif jika
terjadi serangan nukleofilik.
Aldehida dan keton
bereaksi dengan alkohol dengan adanya katalis asam dan menghasilkan asetal
dan ketal sebagai produk,
Reaksi adisi ini juga diatur oleh kesetimbangan yang biasanya terjadi di sisi senyawa karbonil. Dengan adanya alkohol berlebih, reaksi yang dikatalisasi asam dengan aldehida atau keton melampaui tahap hemiasetal
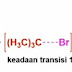
Langkah kedua dapat
disebut sebagai reaksi substitusi S N 1
( pusat sp 3 )
Setiap langkah bisa
dibalik. Seluruh urutan reaksi dari senyawa karbonil ke asetal merupakan
proses kesetimbangan. Dengan memanipulasi kondisi reaksi, kesetimbangan
dapat digeser ke kanan atau ke kiri:
Pembentukan asetal /
ketal membutuhkan alkohol yang berlebihan
Hidrolisis asetal /
ketal membutuhkan banyak air
1,2-Ethanediol (glikol) dan diol serupa bereaksi dengan aldehida dan keton dengan adanya sejumlah katalitik asam untuk membentuk asetal siklik dan ketal:
Sifat penting dari asetal dan ketal adalah kelembaman relatifnya terhadap basa, pereaksi Grignard, zat pereduksi hidrida dan nukleofil lainnya.
Setengah-asetal dan
setengah-ketal biasanya tidak dapat diisolasi. Setengah-asetal atau
setengah-ketal dapat diisolasi dari hidroksi aldehida atau hidroksi keton jika
penutupan cincin mengarah pada pembentukan cincin beranggota lima atau enam.
PERMASALAHAN :
1. Jelaskan bagaimana OH- bisa menjadi nukleofil yang lebih baik daripada H2O? apa yang menjaadi faktor tersebut? apakah ada sifat khusus yang dimiliki OH-?
2. Aldehida dan keton bereaksi dengan alkohol dengan adanya katalis asam dan menghasilkan asetal dan ketal sebagai produk. bagaimana cara memperoleh aseal dalam jumlah yang banyak?
3. Apa yang menjadi pengaturan yang sangat berpengaruh pada mekanisme reaksi keton?







Baiklah saya Rizki Haryati NIM A1C119004 akan mencoba menjawab permasalahan nomor 2.
BalasHapusMenurut saya jika kita ingin agar produk asetal lebih banyak maka dilakukan dengan cara menambah alkohol atau membuang air yang terbentuk.
Terimakasih
Baiklah Saya Aufa Hasnita NIM A1C119040 mencoba menjawab permasalahan nomor 3
BalasHapusketon lebih stabil daripada aldehid. Suatu keton dengan dua gugus R lebih stabil dibandingkan suatu aldehid yang hanya memiliki satu gugus R. Reaktivitas aldehid dan keton dalam reaksi adisi sebagian disebabkan oleh banyak nya muatan positif pada karbon karbonil. Makin besar muatan positif itu akan semakin reaktif. Bila muatan positif parsial ini tersebar ke seluruh molekul maka senyawa karbonil itu lebih stabil dan kurang reaktif. Sehingga pada reaksi adisi ini aldehid lebih stabil dibandingkan keton
Terima kasih semoga membantu
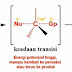
Baiklah, saya Riska Indriyani NIM A1C119091 akan menjawab permasalah nomor 1.
BalasHapusFaktor yang mempengaruhi adalah faktor kestabilan reaksinyanya. Ketika nuklofil OH menyerang karbokation maka OH akan berikatan dengan atom C sementara H2O akan sama seperti OH, dimana atom C akan mengikat H2O namun dalam kondisi tersenut reaksi akan mengalami ketidak stabilan sehingga nantinya dalam keadaan transisi dengan sendirinya H2O akan terlepas dari atom C. Adapun OH memiliki sifat khusus yaitu OH merupakan nukleofil sangat kuat.