MEKANISME REAKSI POKSIDASI PDA SENYAWA ORGANIK
Oksidasi berbagai jenis alkohol
Larutan natrium atau kalium dikromat (VI) yang diasamkan dengan asam sulfat
encer biasanya menjadi zat pengoksidasi yang digunakan dalam reaksi ini. Jika
terjadi oksidasi, larutan jingga yang mengandung ion dikromat (VI) direduksi
menjadi larutan hijau yang mengandung ion kromium (III). Persamaan
setengah elektron untuk reaksi ini adalah
Cr2O2−7+14H++6e−→2Cr3++7H2O
Senyawa pengoksidasi
- K 2 Cr 2 O 7 kalium
dikromat
- CrO 3 kromium
trioksida
Keduanya digunakan bersama dengan H2SO4, H2O
- alkohol primer→ Asam
karboksilat
- alkohol sekunder→ Keton
- alkohol tersier→ Tidak ada
reaksi
Alkohol primer
Alkohol primer dapat dioksidasi menjadi aldehida atau asam karboksilat
tergantung pada kondisi reaksi. Dalam kasus pembentukan asam karboksilat,
alkohol pertama-tama dioksidasi menjadi aldehida yang kemudian dioksidasi lebih
lanjut menjadi asam.
Oksidasi penuh menjadi asam
karboksilat
Perlu digunakan oksidator berlebih dan memastikan bahwa aldehida
yang terbentuk sebagai produk setengah jalan tetap berada dalam
campuran. Alkohol dipanaskan di bawah refluks dengan oksidator
berlebih. Ketika reaksi selesai, asam karboksilat
didistilasi. Persamaan lengkap untuk oksidasi etanol menjadi asam etanoat
adalah:
3CH3CH2OH+2Cr2O2−7+16H+→3CH3COOH+4Cr3++11H2O
Inilah yang terjadi di tahap kedua:
Alkohol sekunder
Alkohol sekunder dioksidasi menjadi keton. Misalnya, jika dipanaskan
alkohol sekunder propan-2-ol dengan larutan natrium atau kalium dikromat (VI)
yang diasamkan dengan asam sulfat encer, akan didapatkan propanon. Reaksi dengan
kondisi reaksi tidak membuat perbedaan apa pun pada produk. Menggunakan
versi persamaan sederhana dan menunjukkan hubungan antara struktur:
Jika kembali pada tahap kedua dari reaksi alkohol primer, akan terlihat
bahwa oksigen "ditempatkan di" antara karbon dan hidrogen dalam gugus
aldehida untuk menghasilkan asam karboksilat. Dalam kasus ini, tidak ada
hidrogen seperti itu dan reaksinya tidak akan berlanjut.
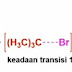
Alkohol tersier
Alkohol tersier tidak teroksidasi oleh larutan natrium atau kalium dikromat
(VI) yang diasamkan tidak ada reaksi apa pun. Jika dilihat apa yang
terjadi dengan alkohol primer dan sekunder, akan terlihat bahwa oksidator
melepaskan hidrogen dari gugus -OH, dan hidrogen dari atom karbon terikat pada
-OH. Alkohol tersier tidak memiliki atom hidrogen yang terikat pada karbon
tersebut.
dua atom hidrogen tersebut harus dilepaskan untuk membentuk ikatan rangkap
karbon-oksigen.
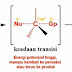
Mekanisme
Contoh
PERMASALAHAN:
1. dijelaskan bahwa "Perlu digunakan oksidator berlebih dan memastikan bahwa aldehida yang terbentuk sebagai produk setengah jalan tetap berada dalam campuran" bagaimana reaksi yang terjadi apabila oksidator yang digunakan kurang dari yang sudah dtentukan? tolong jelaskan
2. pada tahap kedua dari reaksi alkohol primer, oksigen ditempatkan di antara karbon dan hidrogen dalam gugus aldehida untuk menghasilkan asam karboksilat. tetapi, dalam kasus ini tidak ada hidrogen seperti itu dan reaksinya tidak akan berlanjut. bagaimana caranya agar reaksi dappat berlanjut?
3. Alkohol tersier tidak teroksidasi oleh larutan natrium atau kalium dikromat (VI) yang diasamkan. bagaimana jika Alkohol tersier tersebut di oksidasi dalam suasana basa? apakah bisa terjadi rreaksi?







Baiklah saya Arsita dengan NIM A1C119028 akan mencoba menjawab permasalahan no 3 ,dimana alkohol tersier ini juga tidak dapat dioksidasi dalam suasana basa juga karena alkohol tersier tidak mempunyai atom hidrogen pada atom karbon yang mengandung gugus hidroksil. Karena ketidakadaan atom H pada alkohol tersier ini sehingga tidak mengalami dioksidasi.
BalasHapusTerimakasih
Baiklah, saya Elisa Apulina Br Sitepu NIM: A1C119031, izin untuk menjawab permasalahan no 2.
BalasHapusOksidasi ini tidak langsung dari alkohol primer menjadi asam karboksilat biasanya berlangsung melalui aldehida yang sesuai, yang ditransformasikan melalui aldehida hidrat (R-CH(OH)2) melalui reaksi dengan air apabila tidak ada oksigen ditempatkan di antara karbon dan hidrogen dalam gugus aldehida untuk menghasilkan asam karboksilat. Oksidasi alkohol primer pada tingkat aldehida dimungkinkan dengan melakukan reaksi tanpa adanya air, sehingga tidak ada hidrat aldehida yang dapat terbentuk. Selain itu, agar oksidasi alkohol primer tetap berlanjut dapat dilakukan dengan cara oksidasi langsung alkohol primer menjadi asam karboksilat dapat dilakukan dengan menggunakan: Kalium permanganat (KMnO 4 );
Oksidasi Jones ; PDC di DMF ; Oksidasi Heyns ; Ruthenium tetroxide (RuO 4 ); atau TEMPO .
Terimakasih
Saya Adinda Zahra Apriliya NIM A1C119102 akan menjawab permasalahan no. 1
BalasHapusJika pada reaksi tersebut terjadi kekurangan atau kurangnya oksidator saat akan atau sedang berlangsung maka hal yang terjadi ialah aldehida yang terbentuk akan tidak bercampur dengan baik pada produk. Sehingga sulit untuk bereaksi selanjutnya